Equipe 5 – Christian POÜS
Mécanismes cellulaires et moléculaires de l’adaptation au stress
Activités de recherche
Notre équipe étudie les mécanismes moléculaires et cellulaires qui permettent l’adaptation des cellules épithéliales humaines à différents stress qui peuvent être rencontrés au sein de l’organisme, et notamment au niveau du foie. Nous étudions comment ses processus sont coordonnés dans l’espace et dans le temps et comment une adaptation excessive peut favoriser une survie cellulaire nocive pour l’individu.
Actuellement nous travaillons sur 2 grands axes :
– Le rôle du cytosquelette et des organelles lors de stress hépatiques.
– L’étude des glycoprotéines circulantes produites par le foie dans les maladies congénitales de la glycosylation (CDG).
Dans les 2 axes, notre objectif général est d’identifier de nouveaux biosenseurs/biomarqueurs de stress et cibles/outils thérapeutiques.
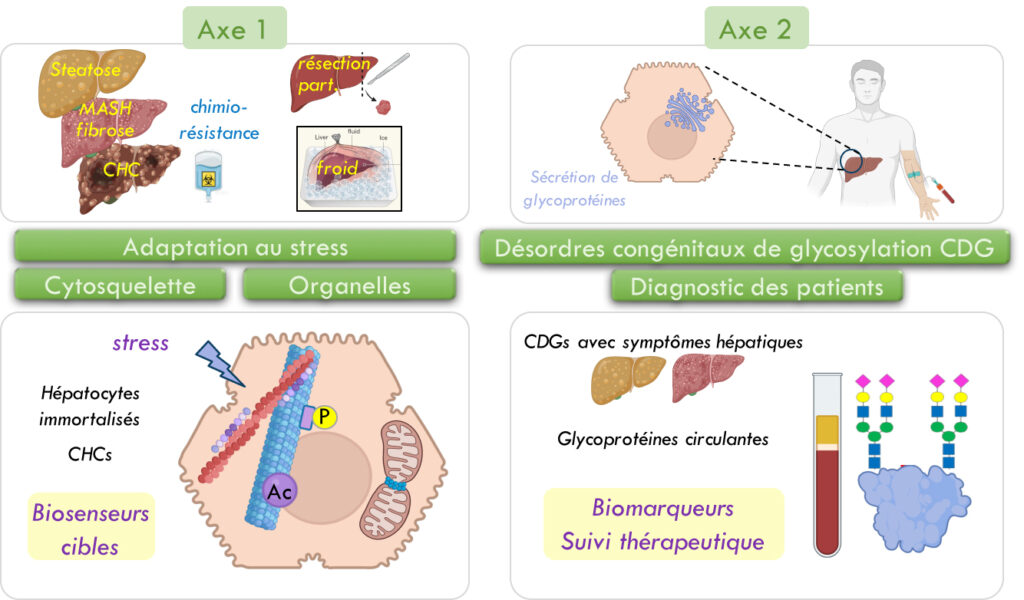
Les cellules du foie sont soumises à des stress infectieux, métaboliques, ioniques, mécaniques, thermiques, médicamenteux ou environnementaux.
On retrouve ainsi du stress oxydant (lié au vieillissement ou à des maladies), du stress osmotique et ionique, la privation en oxygène ou en nutriments (ischémie, cancer), l’accumulation de lipides (stéatose), la compression (fibrose, MASH), l’hypothermie (conservation des greffons), les chimiothérapies anticancéreuses (médicament), les nanoparticules (environnement), du stress Golgien (CDGs), ect.
Les thématiques
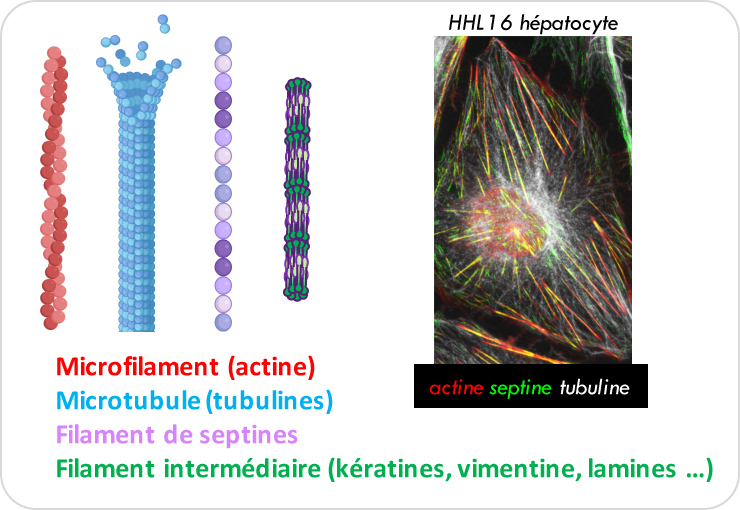
Le cytosquelette : un senseur de stress et médiateur moléculaire des réponses cellulaires
Les cellules humaines possèdent un cytosquelette, une structure dynamique et complexe, qui intervient dans la forme 3D cellulaire, la rigidité, la polarité, l’adhérence, la division, la migration mais aussi la détection et la réponse aux stresses cellulaires.
Le cytosquelette est constitué de quatre composants principaux, qui sont les microfilaments d’actine, les microtubules, les filaments intermédiaires et les filaments de septine.
Ces filaments peuvent interagirent entre eux et sont régulés par de nombreuse protéines, incluant des modificateurs post-traductionnels, pour assurer les multiples fonctions physiologiques mais aussi pour s’adapter à différents stress cellulaires.
Schéma : B. BENOIT (Biorender) et image : A. BAILLET
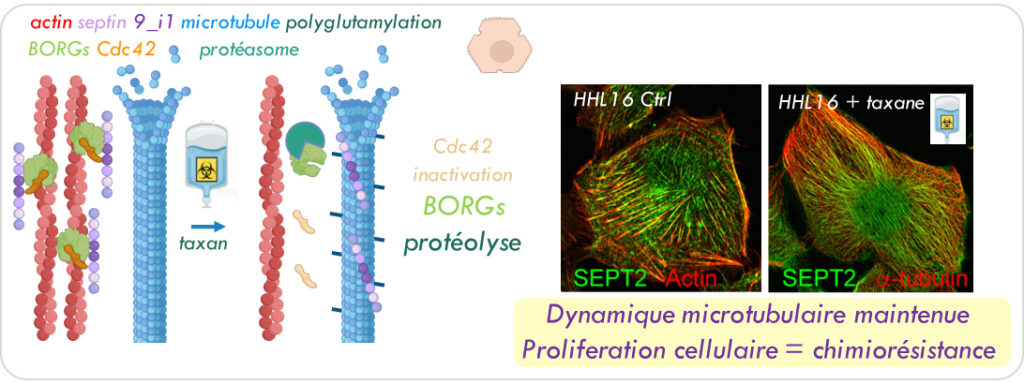
Relocalisation des septines et chimiorésistance aux taxanes
Les taxanes sont des déstabilisateurs connus des microtubules utilisés pour le traitement des cancers du sein, de l’ovaire et de la prostate. Leur efficacité avérée est cependant limitée par des risques de chimiorésistances innées ou acquises.
Nous avons révélé que lors de résistance aux taxanes, les filaments de septines se relocalisent des fibres de stress d’actine vers les microtubules. Ce remaniement général du cytosquelette requiert la présence de l’isoforme 1 de la septine 9 et est associé à la polyglutamylation de la tubuline, pour préserver la dynamique des microtubule, la prolifération cellulaire et donc la chimiorésistance.
Le rôle précoce de l’inactivation de Cdc42 et de la dégradation des protéines BORGs par le protéasome dans ce remaniement, ouvre des perspectives pour développer de nouveaux biomarqueurs de la chimiorésistance. La découverte de ce mécanisme de résistance révèle de nouvelles cibles thérapeutiques potentielles pour éventuellement permettre une utilisation plus générale des taxanes, comme par exemple dans des cancers agressifs et multirésistants tels que les hépatocarcinomes (CHCs) .
Contact : Dr Anita BAILLET, Pr Christian POÜS
Revues : Baillet et al., Journal of Cell Science 2021, Benoit et al. Frontiers in Cell and Developmental Biology 2023
Schéma : B. BENOIT (Biorender), image : B. BAILLET
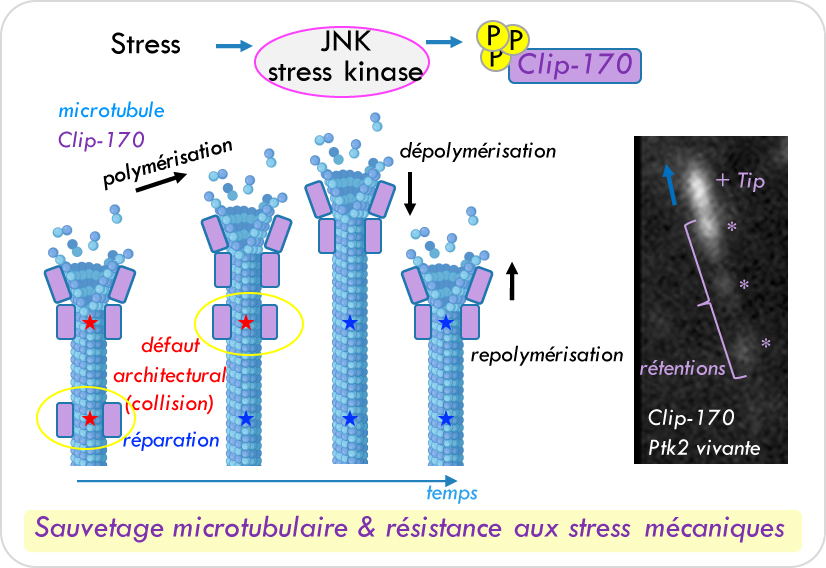
Kinase de stress JNK et dynamique microtubulaire
La kinase de stress JNK est connue pour stabiliser les microtubules dans les neurones et pour réguler le transport moléculaire en phosphorylant des protéines microtubulaires, incluant des moteurs moléculaires.
Nous avons montré que JNK régule aussi la dynamique microtubulaire des cellules épithéliales, en phosphorylant CLIP-170 sur 3 sites consensus (T25, T45 et S147). CLIP-170 est une protéine qui se lie à l’extrémité « plus » en croissance des microtubules (+TIP) et forme des points de rétention transitoire à l’arrière des comètes, au niveau des défauts microtubulaires. Cette protéine a deux fonctions connues, l’une dans le recrutement sur l’extrémité ‘plus’ des microtubules du moteur moléculaire Dynéine associé à ses cargaisons et l’autre dans la stimulation des évènement de sauvetage (repolymérisation) des microtubules.
En condition de stress (antibiotique, osmotique ou UVC), la protéine CLIP-170 est phosphorylée par JNK et devient un meilleur facteur de sauvetage, se retrouvant plus fréquemment mais moins longtemps au niveau des futurs sites de sauvetage. Ceci révèle que CLIP-170 pourrait être un senseur de stress microtubulaire, éventuellement s’associant aux défauts générés lors de la polymérisation pour initier leur réparation et marquer à cet endroit les futurs sites de sauvetage.
JNK est donc un stimulateur du sauvetage microtubulaire qui pourrait participer dans la résistance aux altérations mécaniques du cytosquelette.
Contact : Dr Béatrice BENOIT, Dr Antoine PILON, Pr Christian POÜS
Revues : Benoit et al., International Journal of Molecular Sciences 2021
Schéma : B. BENOIT (Biorender), image : B. BENOIT
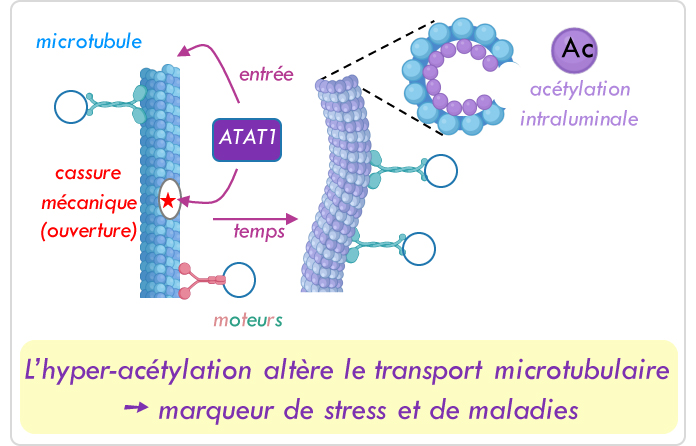
Acétylation des microtubules
L’acétylation des microtubules sur la lysine 40 (K40) requiert l’acétyl-transférase alphaTAT1/Mec17 pour réguler la dynamique microtubulaire, la rigidité des microtubules et l’activité des transporteurs moléculaires.
Nous avons montré que l’hyper-acétylation des microtubules est une réponse fréquente à différents stress, retrouvée aussi dans des maladies telles que l’obésité cardiaque, la réactivation virale d’Epstein-Barr par échappement à l’immunité innée et la paraplégie spastique familiale.
Dans ces exemples, cette modification post-traductionnelle altère l’import du glucose, le transport mitochondrial ou neuronal, mais aussi la fission mitochondriale et la mitophagie.
L’acétylation peut donc être utilisée comme un marqueur de stress cellulaire, mais aussi envisagée comme une nouvelle cible thérapeutique.
Contact : Dr Daniel PERDIZ , Pr Christian POÜS
Publications : Mackeh et al., The Journal of Biological Chemistry 2014, Perdiz et al., Cellular Signaling 2017, Plaud et al., Disease Models & Mechanisms 2018, Glon et al., PLOS Pathogens 2021, Renguet et al., Heart & Circulatory Physiology 2022
Schéma : B. BENOIT (Biorender)
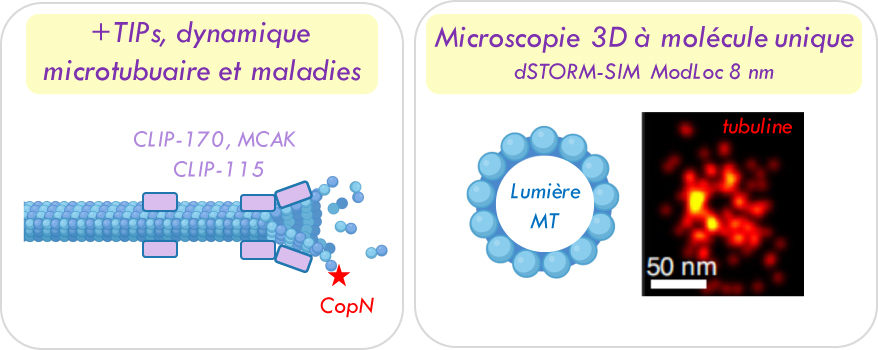
Protéines +TIPs et dynamique microtubulaire
Les protéines +TIPs sont des protéines qui s’associent avec les extrémités ‘plus’ des microtubules en croissance. Nous nous sommes intéressés dans des contextes de maladies aux protéines CLIP-170, CLIP-115, CLASP, MCAK, mais aussi à la protéine bactérienne CopN qui coiffe ces extrémités et inhibe la nucléation microtubulaire.
Nous utilisons la microscopie à haute résolution pour imager la structure du cytosquelette.
Contact : Dr Béatrice BENOIT, Dr Anita BAILLET, Pr Christian POÜS
Publications : Froidevaux-Klipfel et al., Oncotarget 2015, Targa et al., Cell Death & Disease 2019, Campanacci et al., PNAS 2019, Ha et al., Nature 2025, Jouchet et al., Nature Photonics 2021, Jouchet et al., ,Philosophical Transaction Royal Society 2022
Review : Benoit & Poüs, Journal of Cell Biology 2019
Schéma : B. BENOIT (Biorender), image : P. JOUCHET
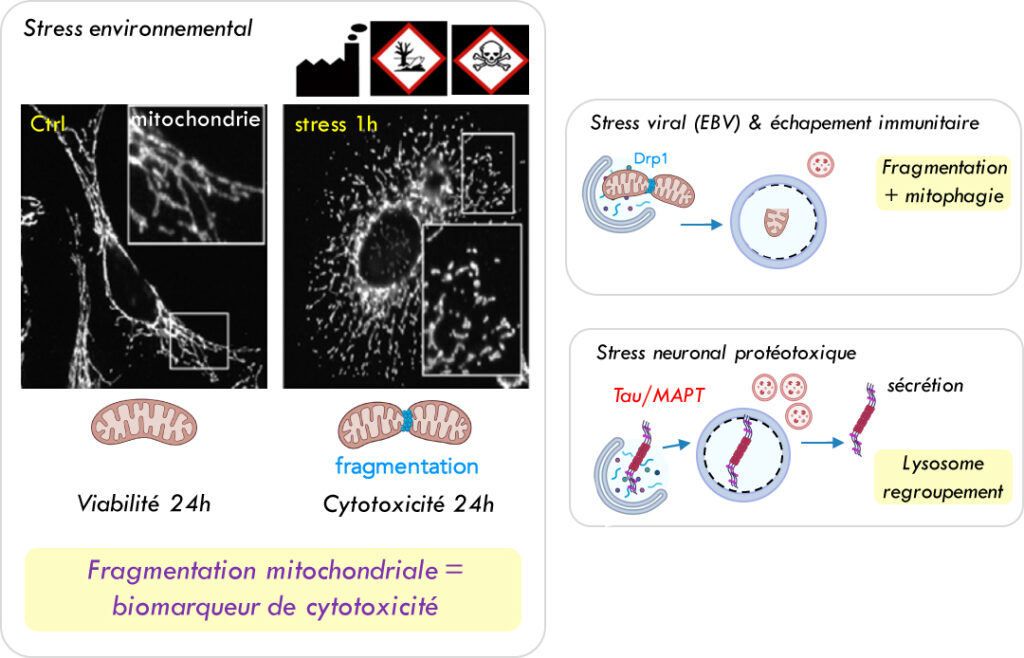
Mitochondries, lysosomes et stress
Les mitochondries et les lysosomes sont non seulement transportés par les microtubules, mais leur dynamique (fusion, fission) et activité dépendent aussi du cytosquelette.
La fragmentation des mitochondries et l’agrégation protéiques sont des marqueurs précoces de stress qui peuvent induire de l’autophagie pour que ces entités cytotoxiques soit dégradées et recyclées par les lysosomes. Des dérégulations de ces processus sont retrouvées dans des maladies.
Contact : Dr Daniel PERDIZ, Pr Christian POÜS
Publications : Perdiz et al., Cellular Signaling 2017, Perdiz et al., Chemosphere 2019, Glon et al., PLOS Pathogens 2021, Vilmen et al., Autophagy 2021
Chambraud et al., Autophagy 2021
Schéma : B. BENOIT (Biorender), image : D. PERDIZ
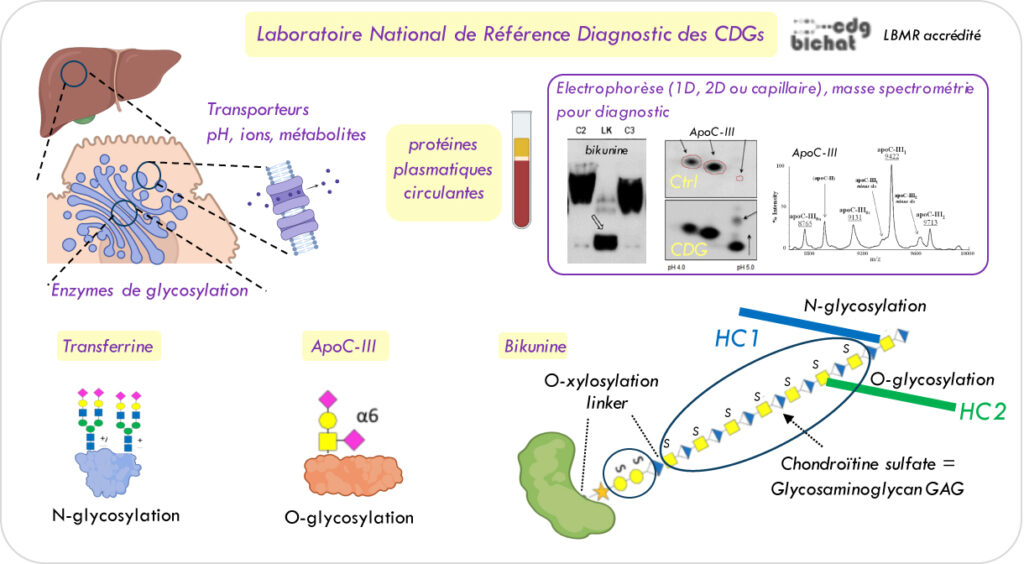
Les biomarqueurs circulants des CDGs : des glycoprotéines poly-modifiées dans l’appareil de Golgi hépatocytaire
Les désordres congénitaux de glycosylation (CDGs) sont un groupe de maladies rares causées par des défauts de glycosylation hérités. Les patients présentent de nombreux symptômes plus ou moins sévères qui varient d’un individu à l’autre, rendant le diagnostic difficile.
La glycosylation consiste en l’assemblage et l’ajout de chaînes saccharidiques, appelées glycanes, sur des protéines ou des lipides. Elle nécessite l’activité de nombreuses enzymes, dont beaucoup sont localisées dans l’appareil de Golgi et requièrent le bon fonctionnement de ce compartiment et des transporteurs/canaux associés.
Les molécules glycosylées sont fréquemment adressées à la membrane plasmique des cellules ou sécrétées dans le milieu extra-cellulaire. On retrouve donc de nombreuses protéines glycosylées dans les matrices extra-cellulaires, mais aussi dans le sang, l’urine ou la salive. Parmi les glycoprotéines circulantes sanguines, synthétisées par les hépatocytes au niveau du foie, la Transferrine, l’ApoC-III et la Bikunine sont facilement accessibles pour rechercher des défauts de glycosylation lors du diagnostic des patients porteurs de CDG ou LK (Linkéropathie).
Contact : Dr Arnaud BRUNEEL, Pr Christian POÜS
https://www.cdg-bichat.com/
CCA 2018, Brain 2022, Nature Comm 2018, Hum Mut 2021
Revues : BBA Gene Subj 2020, Gene 2021
Schéma : B. BENOIT (Biorender), image : A. BRUNEEL
Les gènes altérés dans les CDGs
Des anomalies de glycosylation sont observées lorsque le métabolisme/transport des sucres est altéré (mannose phosphate isomérase MPI, phosphomannomutase PMM2 ou glucose G6PT transporteur), ou lorsque que le transport ionique et le pH golgien sont affectés (Mn2+/H+ TMEM165 transporteur, V-ATPase pompe à proton).
Suivant les mutations, les patients présentent des défauts hépatiques plus ou moins sévères, avec des taux de transaminases élevées et des troubles de la coagulation (G6PT, TMEM65, V-ATPase), des hépatomégalies associées à de la fibrose (MPI) et éventuellement des cholestases et stéatoses qui peuvent évoluer vers de la cirrhose (V-ATPase).
D’autres symptômes sont aussi possibles, notamment des symptômes cérébraux et/ou osseux (PAPS SLC35B2 transporteur affectant la sulfation de protéoglycanes de la matrice extra-cellulaire, pompe V-ATPase, Ca2+ SLC10A7 transporteur de la membrane plasmique, PMM2 phosphomannomutase, Mn2+/H+ TMEM165 transporteur).
La prise en charge médicale repose sur l’utilisation des marqueurs hépatiques circulants (Transferrine, ApoC-III et Bikunine) pour orienter le diagnostic du type de CDG puis l’analyse génétique.
Pour les patients MPI ou TMEM65, des supplémentations en mannose ou Mn2+/galactose respectivement permettent de restaurer un niveau de glycosylation normal et d’atténuer les symptômes cliniques.

Mol Gen Met 2018, CCA 2021
Revues : JJMD 2020 Guideline, PNDS protocole national diagnostic et soin, The Conversation 2024
Schéma : B. BENOIT (Biorender), image : A. BRUNEEL
Membres de l’équipe
EnseignaNts-chercheurs

Pr Christian POÜS
PU-PH
Faculté Pharmacie
Université Paris-Saclay
AP-HP Biochimie Antoine-Béclère
christian.pous@universite-paris-saclay.fr

Pr Antoinette LEMOINE
PU-PH
Oncogénétique
Université Paris-Saclay
AP-HP Biochimie
Paul-Brousse
antoinette.lemoine@universite-paris-saclay.fr

Dr Anita BAILLET
MCF
Faculté Pharmacie
Université Paris-Saclay
anita.baillet@universite-paris-saclay.fr

Dr Arnaud BRUNEEL
MCU-PH
Faculté Pharmacie
Université Paris-Saclay
AP-HP Biochimie
Bichat Claude-Bernard
arnaud.bruneel@universite-paris-saclay.fr

Dr Béatrice BENOIT
MCF
Faculté Pharmacie
Université Paris-Saclay
beatrice.benoit@universite-paris-saclay.fr

Dr Séverine LORIN
MCF
Faculté Pharmacie
Université Paris-Saclay
severine.lorin@universite-paris-saclay.fr

Dr Najet MEJDOUBI-CHAREF
MCF
Faculté Pharmacie
Université Paris-Saclay
najet.mejdoubi-charef@universite-paris-saclay.fr

Dr Daniel PERDIZ
MCF
UFR Pharmacie
Université Paris-Saclay
daniel.perdiz@universite-paris-saclay.fr

Dr Antoine PILON
MCU-PH
UFR Pharmacie
Université Paris-Saclay
AP-HP Biochimie
Saint-Antoine
antoine.pilon@universite-paris-saclay.fr

PersonNels techniqueS

Isabelle CANTALOUBE
Assistante ingénieure
UFR Pharmacie
Université Paris-Saclay
isabelle.cantaloube@universite-paris-saclay.fr

Ameetha RATIER
Technicienne
UFR Pharmacie
Université Paris-Saclay
ameetha.ratier@universite-paris-saclay.fr

Leila DJAMBAE
Agent technique CDD
UFR Pharmacie
Université Paris-Saclay
leila.djambae@universite-paris-saclay.fr

Hadidja MDAHOMA
Agent technique CDD
UFR Pharmacie
Université Paris-Saclay
hadidja.mdahoma@universite-paris-saclay.fr
Masters, doctorants et post-doctorants

Samra OUARAS
Doctorante
ED ITFA
Université Paris-Saclay
AP-HP Biochimie Antoine-Béclère
samra.ouaras@universite-paris-saclay.fr
anciens membres

Elise JACQUIN
MCF
2020-2023
Dr Jocelyne HAMELIN
MCU-PH
2015-2024

Dr Maya TALANTIKE
Postdoctorante Saclay
2017-2018

Dr Dalal DOUAIHY
Postdoctorante Saclay
2018-2019

Benjamin TARGA
Doctorant
ED 569 ITFA
2013-2016

Hélène HENRIE
Doctorante
ED 569 ITFA
2014-2017

Joelle SALAMEH
Doctorante
ED 569 ITFA
2017-2021

Walid HAOUARI
Doctorant
ED 569 ITFA
2018-2021

Mélanie QUESNOIST
Doctorante
2007

Julien GUSTINIANI
Doctorant
2008

Vanessa DAIRE
Doctorante
2009

Camille GEERAERT
Doctorante
2010

Laurence FROIDEVAUX-KLIPFEL
Doctorante
2011

Rafah MACKEH
Doctorante
2013

Claude MARIETTE
Agent technique

Mariem KHAMARI
Agent technique

Théo PUTIGNY
Agent technique

Jennifer JOACHIM
Agent technique

Ingrid LEROY-GORI
Technicienne

Dominique LIGARIUS
Agent technique

Alexis VANDENBERGHE
Agent technique

Bamba TRAORE
Agent technique
départ 2022

Sara MERABET
Agent technique
départ 2022
Publications
2023 – FACULTE PHARMACIE
- “Hide and seek »: Misleading transferrin variants in PMM2-CDG complicate diagnostics. Raynor A, Bruneel A, Vermeersch P, Cholet S, Friedrich S, Eckenweiler M, Schumann A, Hengst S, Tuncel AT, Fenaille F, Thiel C, Rymen D. Proteomics Clin Appl. 2023 Oct 24:e2300040. doi: 10.1002/prca.202300040. Online ahead of print.PMID: 37876147
- Association between acute complications in PMM2-CDG patients and haemostasis anomalies: Data from a multicentric study and suggestions for acute management. Wicker C, Roux CJ, Goujon L, de Feraudy Y, Hully M, Brassier A, Bérat CM, Chemaly N, Wiedemann A, Damaj L, Abi-Warde MT, Dobbelaere D, Roubertie A, Cano A, Arion A, Kaminska A, Da Costa S, Bruneel A, Vuillaumier-Barrot S, Boddaert N, Pascreau T, Borgel D, Kossorotoff M, Harroche A, de Lonlay P. Mol Genet Metab. 2023 Jul 31;140(3):107674. doi: 10.1016/j.ymgme.2023.107674. Online ahead of print.PMID: 37542768
- MAGT1 deficiency in XMEN disease is associated with severe platelet dysfunction and impaired platelet glycoprotein N-glycosylation. Kauskot A, Mallebranche C, Bruneel A, Fenaille F, Solarz J, Viellard T, Feng M, Repérant C, Bordet JC, Cholet S, Denis CV, McCluskey G, Latour S, Martin E, Pellier I, Lasne D, Borgel D, Kracker S, Ziegler A, Tuffigo M, Fournier B, Miot C, Adam F. J Thromb Haemost. 2023 May 18:S1538-7836(23)00420-8. doi: 10.1016/j.jtha.2023.05.007. Online ahead of print.PMID: 37207862
- High CDT without clinical context: Beware of the variant. Lebredonchel E, Raynor A, Bruneel A, Peoc’h K, Klein A. Clin Chim Acta. 2023 Apr 1;544:117333. doi: 10.1016/j.cca.2023.117333. Epub 2023 Apr 6.PMID: 37030568
- SORD-related peripheral neuropathy in a French and Swiss cohort: Clinical features, genetic analyses, and sorbitol dosages. Pons N, Fernández-Eulate G, Pegat A, Théaudin M, Guieu R, Ripellino P, Devedjian M, Mace P, Masingue M, Léonard-Louis S, Petiot P, Roche P, Bernard E, Bouhour F, Good JM, Verschueren A, Grapperon AM, Salort E, Grosset A, Chanson JB, Nadaj-Pakleza A, Bédat-Millet AL, Choumert A, Barnier A, Hamdi G, Lesca G, Prieur F, Bruneel A, Latour P, Stojkovic T, Attarian S, Bonello-Palot N. Eur J Neurol. 2023 Jul;30(7):2001-2011. doi: 10.1111/ene.15793. Epub 2023 Apr 4.PMID: 36943151
- Quantitation of 10 antibiotics in plasma: Sulfosalicylic acid combined with 2D-LC-MS/MS is a robust assay for beta-lactam therapeutic drug monitoring. Palayer M, Chaussenery-Lorentz O, Boubekeur L, Urbina T, Maury E, Maubert MA, Pilon A, Bourgogne E. J Chromatogr B Analyt Technol Biomed Life Sci. 2023 Apr 15;1221:123685.doi:10.1016/j.jchromb.2023.123685. Epub 2023 Mar 28.PMID: 37023569
- Clinical performance of magnetic resonance imaging and biomarkers for prostate cancer diagnosis in men at high genetic risk. Cussenot O, Renard-Penna R, Montagne S, Ondet V, Pilon A, Guechot J, Comperat E, Hamdy F, Lamb A, Cancel-Tassin G. BJU Int. 2023 Jun;131(6):745-754. doi: 10.1111/bju.15968. Epub 2023 Feb 6.PMID: 36648168
- Reversible atransferrinemia in a patient with chronic enteropathy: is transferrin mandatory for iron transport? Raynor A, Stefanescu C, Bruneel A, Puy H, Peoc’h K, Manceau H. Biochem Med (Zagreb). 2023 Feb 15;33(1):010801. doi: 10.11613/BM.2023.010801. Epub 2022 Dec 15.PMID: 36627980
- Septins as membrane influencers: direct play or in association with other cytoskeleton partners. Benoit B, Poüs C, Baillet A. Front Cell Dev Biol. 2023 Feb 17;11:1112319. doi: 10.3389/fcell.2023.1112319
- Clinically relevant urine creatinine underestimation in the low concentration range on the Siemens Dimension Vista®. Raynor A, Raulet-Bussian C, Robert-Mercier T, Bruneel A, Vidal-Petiot E, Flamant M, Boutten A. Clin Biochem. 2023 Jan;111:87-90. doi: 10.1016/j.clinbiochem.2022.10.013. Epub 2022 Nov 8.PMID: 36368568
2023 – CHB
2022 – FACULTE PHARMACIE
- N-Glycosylation Deficiency Reduces the Activation of Protein C and Disrupts Endothelial Barrier Integrity. Pascreau T, Saller F, Bianchini EP, Lasne D, Bruneel A, Reperant C, Foulquier F, Denis CV, De Lonlay P, Borgel D. Thromb Haemost. 2022 Sep;122(9):1469-1478. doi: 10.1055/s-0042-1744378. Epub 2022 Jun 19.PMID: 35717947
- Lab-in-droplet: From glycan sample treatment toward diagnostic screening of congenital disorders of glycosylation. Liénard-Mayor T, Bricteux C, Bendali A, Tran NT, Bruneel A, Taverna M, Mai TD. Anal Chim Acta. 2022 Aug 15;1221:340150. doi: 10.1016/j.aca.2022.340150. Epub 2022 Jul 11.PMID: 35934380
- V-ATPase is a universal regulator of LC3-associated phagocytosis and non-canonical autophagy. Hooper KM, Jacquin E, Li T, Goodwin JM, Brumell JH, Durgan J, Florey O. J Cell Biol. 2022 Jun 6;221(6):e202105112. doi: 10.1083/jcb.202105112. Epub 2022 May 5.PMID: 35511089
- Increased carbohydrate deficient transferrin: Whisky or candy?. Giguet B, Bruneel A, Vuillaumier Barrot S, Moirand R, Bardou Jacquet E. JHEP Rep. 2022 Apr 20;4(7):100494. doi: 10.1016/j.jhepr.2022.100494. eCollection 2022 Jul.PMID: 35647502
- α-Tubulin acetylation on Lysine 40 controls cardiac glucose uptake. Renguet E, De Loof M, Fourny N, Ginion A, Bouzin C, Poüs C, Horman S, Beauloye C, Bultot L, Bertrand L. Am J Physiol Heart Circ Physiol. 2022 Apr 29. doi: 10.1152/ajpheart.00664.2021. Online ahead of print. PMID: 35486479
- Essential role of hyperacetylated microtubules in innate immunity escape orchestrated by the EBV-encoded BHRF1 protein. Glon D, Vilmen G, Perdiz D, Hernandez E, Beauclair G, Quignon F, Berlioz-Torrent C, Maréchal V, Poüs C, Lussignol M, Esclatine A. PLoS Pathog. 2022 Mar 11;18(3):e1010371. doi: 10.1371/journal.ppat.1010371. eCollection 2022 Mar. PMID: 35275978
- Biallelic variants in SLC35B2 cause a novel chondrodysplasia with hypomyelinating leukodystrophy. Guasto A, Dubail J, Aguilera-Albesa S, Paganini C, Vanhulle C, Haouari W, Gorría-Redondo N, Aznal-Sainz E, Boddaert N, Planas-Serra L, Schlüter A, Verdura E, Bruneel A, Rossi A, Huber C, Pujol A, Cormier-Daire V. Brain. 2022 Mar 24:awac110. doi: 10.1093/brain/awac110. Online ahead of print. PMID: 35325049
- Time-modulated excitation for enhanced single-molecule localization microscopy. Jouchet P, Poüs C, Fort E, Lévêque-Fort S. Philos Trans A Math Phys Eng Sci. 2022 Apr 4;380(2220):20200299. doi: 10.1098/rsta.2020.0299. Epub 2022 Feb 14. PMID: 35152758
- High levels of HPV16-L1 antibody but not HPV16 DNA load or integration predict oropharyngeal patient outcome: The Papillophar study. Prétet JL, Dalstein V, Touzé A, Beby-Defaux A, Soussan P, Jacquin É, Birembaut P, Clavel C, Mougin C, Rousseau A, Lacau Saint Guily J; Papillophar Study Group. Clin Exp Med. 2022 Feb 23. doi: 10.1007/s10238-022-00796-2. Online ahead of print. PMID: 35199231
- [Precision intra-assay study in the absence of internal quality control: example of radioimmunoassay of procollagen III peptide]. Laudat A, Pilon A, Vaubourdolle M. Ann Biol Clin (Paris). 2022 Feb 1;80(1):91-95. doi: 10.1684/abc.2022.1700. PMID: 35107065
- Vitamin C improves microvascular reactivity and peripheral tissue perfusion in septic shock patients. Lavillegrand JR, Raia L, Urbina T, Hariri G, Gabarre P, Bonny V, Bigé N, Baudel JL, Bruneel A, Dupre T, Guidet B, Maury E, Ait-Oufella H. Crit Care. 2022 Jan 21;26(1):25. doi: 10.1186/s13054-022-03891-8. PMID: 35062987
- CD4 T cell-intrinsic STING signaling controls the differentiation and effector functions of T H 1 and T H 9 cells. Benoit-Lizon I, Jacquin E, Rivera Vargas T, Richard C, Roussey A, Dal Zuffo L, Martin T, Melis A, Vinokurova D, Shahoei SH, Baeza Garcia A, Pignol C, Giorgiutti S, Carapito R, Boidot R, Végran F, Flavell RA, Ryffel B, Nelson ER, Soulas-Sprauel P, Lawrence T, Apetoh L. J Immunother Cancer. 2022 Jan;10(1):e003459. doi: 10.1136/jitc-2021-003459. PMID: 35091453
- MEK inhibition overcomes chemoimmunotherapy resistance by inducing CXCL10 in cancer cells. Limagne E, Nuttin L, Thibaudin M, Jacquin E, Aucagne R, Bon M, Revy S, Barnestein R, Ballot E, Truntzer C, Derangère V, Fumet JD, Latour C, Rébé C, Bellaye PS, Kaderbhaï CG, Spill A, Collin B, Callanan MB, Lagrange A, Favier L, Coudert B, Arnould L, Ladoire S, Routy B, Joubert P, Ghiringhelli F. Cancer Cell. 2022 Feb 14;40(2):136-152.e12. doi: 10.1016/j.ccell.2021.12.009. Epub 2022 Jan 19. PMID: 35051357
- Delayed inflammation decrease is associated with mortality in Tocilizumab-treated critically ill SARS-CoV-2 patients: A retrospective matched-cohort analysis. Urbina T, Lavillegrand JR, Garnier M, Mekinian A, Pacanowski J, Mario N, Dumas G, Hariri G, Pilon A, Darrivère L, Fartoukh M, Guidet B, Maury E, Leblanc J, Chantran Y, Fain O, Lacombe K, Voiriot G, Ait-Oufella H. Innate Immun. 2022 Jan;28(1):3-10. doi: 10.1177/17534259211064602. Epub 2022 Jan 28. PMID: 35089113
2022 – CHB
2021 – FACULTE PHARMACIE
- Meeting report – the ever-fascinating world of septins. Baillet A, McMurray MA, Oakes PW. J Cell Sci. 2021 Dec 15;134(24):jcs259552. doi: 10.1242/jcs.259552. Epub 2021 Dec 15. PMID: 34910818
- [SORD-related hereditary neuropathies]. Fernández-Eulate G, Bruneel A, Stojkovic T. Med Sci (Paris). 2021 Nov;37 Hors série n° 1:30-31. doi: 10.1051/medsci/2021188. Epub 2021 Dec 8. PMID: 34878391
- High sensitivity capillary electrophoresis with fluorescent detection for glycan mapping. Liénard-Mayor T, Yang B, Tran NT, Bruneel A, Guttman A, Taverna M, Mai TD. J Chromatogr A. 2021 Nov 8;1657:462593. doi: 10.1016/j.chroma.2021.462593. Epub 2021 Oct 2. PMID: 34689907
- Inherited proteoglycan biosynthesis defects-current laboratory tools and Bikunin as a promising blood biomarker. Haouari W, Dubail J, Poüs C, Cormier-Daire V, Bruneel A. Genes (Basel). 2021 Oct 20;12(11):1654.doi:10.3390/genes12111654. PMID: 34828260
- SLC37A4-CDG: New biochemical insights for an emerging congenital disorder of glycosylation with major coagulopathy. Raynor A, Haouari W, Ng BG, Cholet S, Harroche A, Raulet-Bussian C, Lounis-Ouaras S, Vuillaumier-Barrot S, Pascreau T, Borgel D, Freeze HH, Fenaille F, Bruneel A. Clin Chim Acta. 2021 Oct;521:104-106. doi: 10.1016/j.cca.2021.07.005. Epub 2021 Jul 8. PMID: 34245688
- Cytoskeleton and associated proteins: pleiotropic JNK substrates and regulators. Benoit B, Baillet A, Poüs C. Int J Mol Sci. 2021 Aug 4;22(16):8375. doi: 10.3390/ijms22168375. PMID: 34445080
- Cdc42 and its BORG2 and BORG3 effectors control the subcellular localization of septins between actin stress fibers and microtubules. Salameh J, Cantaloube I, Benoit B, Poüs C, Baillet A. Curr Biol. 2021 Sep 27;31(18):4088-4103.e5. doi: 10.1016/j.cub.2021.07.004. Epub 2021 Jul 29. PMID: 34329591
- Decrease of neuronal FKBP4/FKBP52 modulates perinuclear lysosomal positioning and MAPT/Tau behavior during MAPT/Tau-induced proteotoxic stress. Chambraud B, Daguinot C, Guillemeau K, Genet M, Dounane O, Meduri G, Poüs C, Baulieu EE, Giustiniani J. Autophagy. 2021 Nov;17(11):3491-3510. doi: 10.1080/15548627.2021.1875611. Epub 2021 Jan 25. PMID: 33459145
- MAN1B1-CDG: Three new individuals and associated biochemical profiles. Sakhi S, Cholet S, Wehbi S, Isidor B, Cogne B, Vuillaumier-Barrot S, Dupré T, Detleft T, Schmitt E, Leheup B, Bonnet C, Feillet F, Muti C, Fenaille F, Bruneel A. Mol Genet Metab Rep. 2021 Jun 2;28:100775. doi: 10.1016/j.ymgmr.2021.100775. eCollection 2021 Sep. PMID: 34141584
- Normal transferrin patterns in congenital disorders of glycosylation with Golgi homeostasis disruption: apolipoprotein C-III at the rescue! Raynor A, Vincent-Delorme C, Alaix AS, Cholet S, Dupré T, Vuillaumier-Barrot S, Fenaille F, Besmond C, Bruneel A. Clin Chim Acta. 2021 Aug;519:285-290. doi: 10.1016/j.cca.2021.05.016. Epub 2021 May 20. PMID: 34022244
- A mutation in SLC37A4 causes a dominantly inherited congenital disorder of glycosylation characterized by liver dysfunction. Ng BG, Sosicka P, Fenaille F, Harroche A, Vuillaumier-Barrot S, Porterfield M, Xia ZJ, Wagner S, Bamshad MJ, Vergnes-Boiteux MC, Cholet S, Dalton S, Dell A, Dupré T, Fiore M, Haslam SM, Huguenin Y, Kumagai T, Kulik M, McGoogan K, Michot C, Nickerson DA, Pascreau T, Borgel D, Raymond K, Warad D; University of Washington Center for Mendelian Genomics (UW-CMG), Flanagan-Steet H, Steet R, Tiemeyer M, Seta N, Bruneel A, Freeze HH. Am J Hum Genet. 2021 Jun 3;108(6):1040-1052. doi: 10.1016/j.ajhg.2021.04.013. Epub 2021 May 7. PMID: 33964207
- Capillary zone electrophoresis of transferrin and EDTA samples in congenital disorders of glycosylation screening: CaNOt do, really? Raynor A, Raulet-Bussian C, Verel L, Plouviez G, Bruneel A. Clin Chim Acta. 2021 Aug;519:92-93. doi: 10.1016/j.cca.2021.04.013. Epub 2021 Apr 20. PMID: 33891959
- The exon junction complex core factor eIF4A3 is a key regulator of HPV16 gene expression. Meznad K, Paget-Bailly P, Jacquin E, Peigney A, Aubin F, Guittaut M, Mougin C, Prétet JL, Baguet A. Biosci Rep. 2021 Apr 30;41(4):BSR20203488. doi: 10.1042/BSR20203488. PMID: 33760064
- Expanding the phenotype of X-linked SSR4-CDG: Connective tissue implications. Castiglioni C, Feillet F, Barnerias C, Wiedemann A, Muchart J, Cortes F, Hernando-Davalillo C, Montero R, Dupré T, Bruneel A, Seta N, Vuillaumier-Barrot S, Serrano M. Hum Mutat. 2021 Feb;42(2):142-149. doi: 10.1002/humu.24151. Epub 2020 Dec 21. PMID: 33300232
- Guidelines for the use and interpretation of assays for monitoring autophagy (4th edition). Klionsky D, …, Jacquin E, et al. Autophagy. 2021 Jan;17(1):1-382. doi: 10.1080/15548627.2020.1797280. Epub 2021 Feb 8. PMID: 33634751
- BHRF1, a BCL2 viral homolog, disturbs mitochondrial dynamics and stimulates mitophagy to dampen type I IFN induction. Vilmen G, Glon D, Siracusano G, Lussignol M, Shao Z, Hernandez E, Perdiz D, Quignon F, Mouna L, Poüs C, Gruffat H, Maréchal V, Esclatine A. Autophagy. 2021 Jun;17(6):1296-1315. doi: 10.1080/15548627.2020.1758416. Epub 2020 May 13. PMID: 32401605
- Elevated plasma IL-6 and CRP levels are associated with adverse clinical outcomes and death in critically ill SARS-CoV-2 patients: inflammatory response of SARS-CoV-2 patients. Lavillegrand JR, Garnier M, Spaeth A, Mario N, Hariri G, Pilon A, Berti E, Fieux F, Thietart S, Urbina T, Turpin M, Darrivere L, Fartoukh M, Verdonk F, Dumas G, Tedgui A, Guidet B, Maury E, Chantran Y, Voiriot G, Ait-Oufella H. Ann Intensive Care. 2021 Jan 13;11(1):9. doi: 10.1186/s13613-020-00798-x. PMID: 33439360
2021 – CHB
- De novo hepatocellular carcinoma in a non-cirrhotic allograft 27 years after liver transplantation: A case report. El-Domiaty N, Saliba F, Sebagh M, Salloum C, Vibert E, Azoulay D, Hamelin J, Cherqui D, Adam R, Samuel D. Am J Transplant. 2021 May;21(5):1953-1958. doi: 10.1111/ajt.16476. Epub 2021 Jan 23. PMID: 33382179
- Endothelin-1 Exhibiting Pro-Nociceptive and Pro-Peristaltic Activities Is Increased in Peritoneal Carcinomatosis. Greco C, Basso L, Désormeaux C, Fournel A, Demuynck B, Lafendi L, Chapiro S, Lemoine A, Zhu YY, Knauf C, Cenac N, Boucheix C, Dietrich G. Front Pain Res (Lausanne). 2021 Feb 11;2:613187. doi: 10.3389/fpain.2021.613187. eCollection 2021. PMID: 35295482
- A mobile DNA laboratory for forensic science adapted to coronavirus SARS-CoV-2 diagnosis. Touron P, Siatka C, Pussiau A, Follot S, Fritz T, Petit M, Latifa N, Herrmann JL, Rottman M, Lemoine A, Hubac S. Eur J Clin Microbiol Infect Dis. 2021 Jan;40(1):197-200. doi: 10.1007/s10096-020-03989-3. Epub 2020 Jul 14. PMID: 32666482
- Reply to P. Gazzaniga et al. Bouchahda M, Saffroy R, Karaboué A, Hamelin J, Innominato P, Saliba F, Bosselut N, Lemoine A, Lévi F. JCO Precis Oncol. 2021 Nov;5:391-392. doi: 10.1200/PO.20.00465. PMID: 34994602
2020 – FACULTE PHARMACIE
- Long term outcome of MPI-CDG patients on D-mannose therapy. Girard M, Douillard C, Debray D, Lacaille F, Schiff M, Vuillaumier-Barrot S, Dupré T, Fabre M, Damaj L, Kuster A, Torre S, Mention K, McLin V, Dobbelaere D, Borgel D, Bauchard E, Seta N, Bruneel A, De Lonlay P. J Inherit Metab Dis. 2020 Nov;43(6):1360-1369. doi: 10.1002/jimd.12289. Epub 2020 Aug 9. PMID: 33098580
- Serum bikunin isoforms in congenital disorders of glycosylation and linkeropathies. Haouari W, Dubail J, Lounis-Ouaras S, Prada P, Bennani R, Roseau C, Huber C, Afenjar A, Colin E, Vuillaumier-Barrot S, Seta N, Foulquier F, Poüs C, Cormier-Daire V, Bruneel A. J Inherit Metab Dis. 2020 Nov;43(6):1349-1359. doi: 10.1002/jimd.12291. Epub 2020 Aug 7. PMID: 32700771
- CDG biochemical screening: Where do we stand? Bruneel A, Cholet S, Tran NT, Mai TD, Fenaille F. Biochim Biophys Acta Gen Subj. 2020 Oct;1864(10):129652. doi: 10.1016/j.bbagen.2020.129652. Epub 2020 Jun 5. PMID: 32512173
- Consensus guideline for the diagnosis and management of mannose phosphate isomerase-congenital disorder of glycosylation. Čechová A, Altassan R, Borgel D, Bruneel A, Correia J, Girard M, Harroche A, Kiec-Wilk B, Mohnike K, Pascreau T, Pawliński Ł, Radenkovic S, Vuillaumier-Barrot S, Aldamiz-Echevarria L, Couce ML, Martins EG, Quelhas D, Morava E, de Lonlay P, Witters P, Honzík T. J Inherit Metab Dis. 2020 Jul;43(4):671-693. doi: 10.1002/jimd.12241. Epub 2020 Apr 21. PMID: 32266963
- Stress-induced phosphorylation of CLIP-170 by JNK promotes microtubule rescue. Henrie H, Bakhos-Douaihy D, Cantaloube I, Pilon A, Talantikite M, Stoppin-Mellet V, Baillet A, Poüs C, Benoit B. J Cell Biol. 2020 Jul 6;219(7):e201909093. doi: 10.1083/jcb.201909093. PMID: 32491151
2020 – CHB
- Undetectable RAS-Mutant Clones in Plasma: Possible Implication for Anti-EGFR Therapy and Prognosis in Patients With RAS-Mutant Metastatic Colorectal Cancer. Bouchahda M, Saffroy R, Karaboué A, Hamelin J, Innominato P, Saliba F, Lévi F, Bosselut N, Lemoine A. JCO Precis Oncol. 2020 Sep 16;4:PO.19.00400. doi: 10.1200/PO.19.00400. eCollection 2020. PMID: 33015528
- Inequity in access to personalized medicine in France: Evidences from analysis of geo variations in the access to molecular profiling among advanced non-small-cell lung cancer patients: Results from the IFCT Biomarkers France Study. Kembou Nzale S, Weeks WB, Ouafik L, Rouquette I, Beau-Faller M, Lemoine A, Bringuier PP, Le Coroller Soriano AG, Barlesi F, Ventelou B. PLoS One. 2020 Jul 1;15(7):e0234387. doi: 10.1371/journal.pone.0234387. eCollection 2020. PMID: 32609781
- Outcomes of Patients With Advanced NSCLC From the Intergroupe Francophone de Cancérologie Thoracique Biomarkers France Study by KRAS Mutation Subtypes. Ruppert AM, Beau-Faller M, Debieuvre D, Ouafik L, Westeel V, Rouquette I, Mazières J, Bringuier PP, Monnet I, Escande F, Ricordel C, Merlio JP, Janicot H, Lemoine A, Foucher P, Poudenx M, Morin F, Langlais A, Souquet PJ, Barlesi F, Wislez M. JTO Clin Res Rep. 2020 May 15;1(3):100052. doi: 10.1016/j.jtocrr.2020.100052. eCollection 2020 Sep. PMID: 34589947
- Redox signaling in the pathogenesis of human disease and the regulatory role of autophagy. Pervaiz S, Bellot GL, Lemoine A, Brenner C. Int Rev Cell Mol Biol. 2020;352:189-214. doi: 10.1016/bs.ircmb.2020.03.002. Epub 2020 Apr 1. PMID: 32334816
- BRCA1 Promoter Hypermethylation is Associated with Good Prognosis and Chemosensitivity in Triple-Negative Breast Cancer. Jacot W, Lopez-Crapez E, Mollevi C, Boissière-Michot F, Simony-Lafontaine J, Ho-Pun-Cheung A, Chartron E, Theillet C, Lemoine A, Saffroy R, Lamy PJ, Guiu S.
Cancers (Basel). 2020 Mar 30;12(4):828. doi: 10.3390/cancers12040828. PMID: 32235500 - Independent prognostic value of ultra-sensitive quantification of tumor pre-treatment T790M subclones in EGFR mutated non-small cell lung cancer (NSCLC) treated by first/second generation TKI, depends on variant allele frequency (VAF): Results of the French cooperative thoracic intergroup (IFCT) biomarkers France project. Beau-Faller M, Pencreach E, Leduc C, Blons H, Merlio JP, Bringuier PP, de Fraipont F, Escande F, Lemoine A, Ouafik L, Denis M, Hofman P, Lacave R, Melaabi S, Langlais A, Missy P, Morin F, Moro-Sibilot D, Barlesi F, Cadranel J; French Cooperative Thoracic Intergroup (IFCT). Lung Cancer. 2020 Feb;140:19-26. doi: 10.1016/j.lungcan.2019.10.013. Epub 2019 Nov 15. PMID: 31841714
2019 – FACULTE PHARMACIE
- Elevated thrombin generation in patients with congenital disorder of glycosylation and combined coagulation factor deficiencies. Pascreau T, de la Morena-Barrio ME, Lasne D, Serrano M, Bianchini E, Kossorotoff M, Boddaert N, Bruneel A, Seta N, Vicente V, de Lonlay P, Corral J, Borgel D. J Thromb Haemost. 2019 Nov;17(11):1798-1807. doi: 10.1111/jth.14559. Epub 2019 Jul 28. PMID: 31271700
- Integrating mass spectrometry-based plasma (or serum) protein N-glycan profiling into the clinical practice? Bruneel A, Fenaille F. Ann Transl Med. 2019 Sep;7(Suppl 6):S225. doi: 10.21037/atm.2019.08.04. PMID: 31656804
- Insight into microtubule nucleation from tubulin-capping proteins. Campanacci V, Urvoas A, Cantos-Fernandes S, Aumont-Nicaise M, Arteni AA, Velours C, Valerio-Lepiniec M, Dreier B, Plückthun A, Pilon A, Poüs C, Minard P, Gigant B. Proc Natl Acad Sci U S A. 2019 May 14;116(20):9859-9864. doi: 10.1073/pnas.1813559116. Epub 2019 Apr 29. PMID: 31036638
- Long-term follow-up in PMM2-CDG: are we ready to start treatment trials? Witters P, Honzik T, Bauchart E, Altassan R, Pascreau T, Bruneel A, Vuillaumier S, Seta N, Borgel D, Matthijs G, Jaeken J, Meersseman W, Cassiman D, Pascale de L, Morava E. Genet Med. 2019 May;21(5):1181-1188. doi: 10.1038/s41436-018-0301-4. Epub 2018 Oct 8. PMID: 30293989
- Septin 9 has two polybasic domains critical to Septin filament assembly and Golgi Integrity. Omrane M, Camara AS, Taveneau C, Benzoubir N, Tubiana T, Yu J, Guérois R, Samuel D, Goud B, Poüs C, Bressanelli S, Garratt RC, Thiam AR, Gassama-Diagne A. iScience. 2019
Mar 29;13:138-153. doi: 10.1016/j.isci.2019.02.015. Epub 2019 Feb 19. PMID: 30831549 - Early mitochondrial fragmentation is a potential in vitro biomarker of environmental stress. Perdiz D, Oziol L, Poüs C. Chemosphere. 2019 May;223:577-587. doi: 10.1016/j.chemosphere.2019.02.044. Epub 2019 Feb 15. PMID: 30797167
- Septin filament coalignment with microtubules depends on SEPT9_i1 and tubulin polyglutamylation, and is an early feature of acquired cell resistance to paclitaxel. Targa B, Klipfel L, Cantaloube I, Salameh J, Benoit B, Poüs C, Baillet A. Cell Death Dis. 2019 Jan 22;10(2):54. doi: 10.1038/s41419-019-1318-6. PMID: 30670682
- Microtubule reorientation in the blue spotlight: Cutting and CLASPing at dynamic hot spots. Benoit B, Poüs C. J Cell Biol. 2019 Jan 7;218(1):8-9. doi: 10.1083/jcb.201812063. Epub 2018 Dec 20. PMID: 30573524
2019 – CHB
- [Could the publication of new european guidelines change practices in France?]. Robinet A, Aljhni R, Fouassier É, Pham P, Bosselut N, Bergouin E, Lemoine A. Ann Biol Clin (Paris). 2019 Oct 1;77(5):505-513. doi: 10.1684/abc.2019.1477. PMID: 31475911
- Effects in Cancer Cells of the Recombinant l-Methionine Gamma-Lyase from Brevibacterium aurantiacum. Encapsulation in Human Erythrocytes for Sustained l-Methionine Elimination. Machover D, Rossi L, Hamelin J, Desterke C, Goldschmidt E, Chadefaux-Vekemans B, Bonnarme P, Briozzo P, Kopečný D, Pierigè F, Magnani M, Mollicone R, Haghighi-Rad F, Gaston-Mathé Y, Dairou J, Boucheix C, Saffroy R. J Pharmacol Exp Ther. 2019 Jun;369(3):489-502. doi: 10.1124/jpet.119.256537. Epub 2019 Apr 2. PMID: 30940696
- Chronological occurrence of PI3KCA mutations in breast cancer liver metastases after repeat partial liver resection. Ruiz A, Sebagh M, Saffroy R, Allard MA, Bosselut N, Hardoin G, Vasseur J, Hamelin J, Adam R, Morère JF, Lemoine A. BMC Cancer. 2019 Feb 22;19(1):169. doi: 10.1186/s12885-019-5365-2. PMID: 30795751
- CSRP3 mediates polyphenols-induced cardioprotection in hypertension. Oudot C, Gomes A, Nicolas V, Le Gall M, Chaffey P, Broussard C, Calamita G, Mastrodonato M, Gena P, Perfettini JL, Hamelin J, Lemoine A, Fischmeister R, Vieira HLA, Santos CN, Brenner C. J Nutr Biochem. 2019 Apr;66:29-42. doi: 10.1016/j.jnutbio.2019.01.001. Epub 2019 Jan 8. PMID: 30703746
- Several clock genes polymorphisms are meaningful risk factors in the development and severity of cannabis addiction. Saffroy R, Lafaye G, Desterke C, Ortiz-Tudela E, Amirouche A, Innominato P, Pham P, Benyamina A, Lemoine A. Chronobiol Int. 2019 Jan;36(1):122-134. doi: 10.1080/07420528.2018.1523797. Epub 2018 Dec 11. PMID: 30526093
2018 – FACULTE pharMacie
- A mutation in the gene coding for the sialic acid transporter SLC35A1 is required for platelet life span but not proplatelet formation. Kauskot A, Pascreau T, Adam F, Bruneel A, Reperant C, Lourenco-Rodrigues MD, Rosa JP, Petermann R, Maurey H, Auditeau C, Lasne D, Denis CV, Bryckaert M, de Lonlay P, Lavenu-Bombled C, Melki J, Borgel D. Haematologica. 2018 Dec;103(12):e613-e617. doi: 10.3324/haematol.2018.198028. Epub 2018 Aug 16. PMID: 30115659
- Functional differences of short and long isoforms of spastin harboring missense mutation. Plaud C, Joshi V, Kajevu N, Poüs C, Curmi PA, Burgo A. Dis Model Mech. 2018 Sep 10;11(9):dmm033704. doi: 10.1242/dmm.033704. PMID: 30213879
- Serum bikunin is a biomarker of linkeropathies. Bruneel A, Dubail J, Roseau C, Prada P, Haouari W, Huber C, Dupré T, Poüs C, Cormier-Daire V, Seta N. Clin Chim Acta. 2018 Oct;485:178-180. doi: 10.1016/j.cca.2018.06.044. Epub 2018 Jun 30. PMID: 29969625
- SLC10A7 mutations cause a skeletal dysplasia with amelogenesis imperfecta mediated by GAG biosynthesis defects. Dubail J, Huber C, Chantepie S, Sonntag S, Tüysüz B, Mihci E, Gordon CT, Steichen-Gersdorf E, Amiel J, Nur B, Stolte-Dijkstra I, van Eerde AM, van Gassen KL, Breugem CC, Stegmann A, Lekszas C, Maroofian R, Karimiani EG, Bruneel A, Seta N, Munnich A, Papy-Garcia D, De La Dure-Molla M, Cormier-Daire V. Nat Commun. 2018 Aug 6;9(1):3087. doi: 10.1038/s41467-018-05191-8. PMID: 30082715
- Complementarity of electrophoretic, mass spectrometric, and gene sequencing techniques for the diagnosis and characterization of congenital disorders of glycosylation. Bruneel A, Cholet S, Drouin-Garraud V, Jacquemont ML, Cano A, Mégarbané A, Ruel C, Cheillan D, Dupré T, Vuillaumier-Barrot S, Seta N, Fenaille F. Electrophoresis. 2018 Dec;39(24):3123-3132. doi: 10.1002/elps.201800021. Epub 2018 Jul 3. PMID: 29869806
- CCDC115-CDG: A new rare and misleading inherited cause of liver disease. Girard M, Poujois A, Fabre M, Lacaille F, Debray D, Rio M, Fenaille F, Cholet S, Ruel C, Caussé E, Selves J, Bridoux-Henno L, Woimant F, Dupré T, Vuillaumier-Barrot S, Seta N, Alric L, de Lonlay P, Bruneel A. Mol Genet Metab. 2018 Jul;124(3):228-235. doi: 10.1016/j.ymgme.2018.05.002. Epub 2018 May 9. PMID: 29759592
- On-a-chip tryptic digestion of transthyretin: a step toward an integrated microfluidic system for the follow-up of familial transthyretin amyloidosis. Bataille J , Viodé A , Pereiro I , Lafleur JP , Varenne F , Descroix S , Becher F , Kutter JP , Roesch C , Poüs C , Taverna M , Pallandre A , Smadja C , Le Potier I. Analyst. 2018 Feb 26;143(5):1077-1086. doi: 10.1039/c7an01737e. PMID: 29383369
- A capillary zone electrophoresis method for detection of Apolipoprotein C-III glycoforms and other related artifactually modified species. Ruel C, Morani M, Bruneel A, Junot C, Taverna M, Fenaille F, Tran NT. J Chromatogr A. 2018 Jan 12;1532:238-245. doi: 10.1016/j.chroma.2017.12.002. Epub 2017 Dec 5. PMID: 29221866
2018 – CHB
- c-MET Overexpression as a Poor Predictor of MET Amplifications or Exon 14 Mutations in Lung Sarcomatoid Carcinomas. Mignard X, Ruppert AM, Antoine M, Vasseur J, Girard N, Mazières J, Moro-Sibilot D, Fallet V, Rabbe N, Thivolet-Bejui F, Rouquette I, Lantuejoul S, Cortot A, Saffroy R, Cadranel J, Lemoine A, Wislez M. J Thorac Oncol. 2018 Dec;13(12):1962-1967. doi: 10.1016/j.jtho.2018.08.008. Epub 2018 Aug 24. PMID: 30149144
- Rare genetic heterogeneity within single tumor discovered for the first time in colorectal liver metastases after liver resection. Sebagh M, Bosselut N, Santos AD, Allard MA, Ruiz A, Saffroy R, Cherqui D, Vibert E, Castaing D, Adam R, Cunha AS, Lemoine A. Oncotarget. 2018 Apr 24;9(31):21921-21929. doi: 10.18632/oncotarget.25119. eCollection 2018 Apr 24. PMID: 29774112
- Suitability of livers for transplantation when treated by normothermic machine perfusion. Allard MA, Castro-Benitez C, Imai K, Selten J, Lopez A, Sebagh M, Lemoine A, Sa Cunha A, Cherqui D, Castaing D, Vibert E, Adam R. Clin Transplant. 2018 Jun;32(6):e13256. doi: 10.1111/ctr.13256. Epub 2018 May 7. PMID: 29637631
2017 – FACULTE pharMacie
- A Fully Automated Web-Based Program Improves Lifestyle Habits and HbA1c in Patients With Type 2 Diabetes and Abdominal Obesity: Randomized Trial of Patient E-Coaching Nutritional Support (The ANODE Study). Hansel B, Giral P, Gambotti L, Lafourcade A, Peres G, Filipecki C, Kadouch D, Hartemann A, Oppert JM, Bruckert E, Marre M, Bruneel A, Duchene E, Roussel R. J Med Internet Res. 2017 Nov 8;19(11):e360. doi: 10.2196/jmir.7947. PMID: 29117929
- Clinical, laboratory and molecular findings and long-term follow-up data in 96 French patients with PMM2-CDG (phosphomannomutase 2-congenital disorder of glycosylation) and review of the literature. Schiff M, Roda C, Monin ML, Arion A, Barth M, Bednarek N, Bidet M, Bloch C, Boddaert N, Borgel D, Brassier A, Brice A, Bruneel A, Buissonnière R, Chabrol B, Chevalier MC, Cormier-Daire V, De Barace C, De Maistre E, De Saint-Martin A, Dorison N, Drouin-Garraud V, Dupré T, Echenne B, Edery P, Feillet F, Fontan I, Francannet C, Labarthe F, Gitiaux C, Héron D, Hully M, Lamoureux S, Martin-Coignard D, Mignot C, Morin G, Pascreau T, Pincemaille O, Polak M, Roubertie A, Thauvin-Robinet C, Toutain A, Viot G, Vuillaumier-Barrot S, Seta N, De Lonlay P. J Med Genet. 2017 Dec;54(12):843-851. doi: 10.1136/jmedgenet-2017-104903. Epub 2017 Sep 27. PMID: 28954837
- Stress-induced hyperacetylation of microtubule enhances mitochondrial fission and modulates the phosphorylation of Drp1 at 616 Ser. Perdiz D, Lorin S, Leroy-Gori I, Poüs C. Cell Signal. 2017 Nov;39:32-43. doi: 10.1016/j.cellsig.2017.07.020. Epub 2017 Jul 28. PMID: 28757354
- Two-dimensional electrophoresis highlights haptoglobin beta chain as an additional biomarker of congenital disorders of glycosylation. Bruneel A, Habarou F, Stojkovic T, Plouviez G, Bougas L, Guillemet F, Brient N, Henry D, Dupré T, Vuillaumier-Barrot S, Seta N. Clin Chim Acta. 2017 Jul;470:70-74. doi: 10.1016/j.cca.2017.04.022. Epub 2017 Apr 27. PMID: 28457853
- Biotin interferes with free thyroid hormone and thyroglobulin, but not TSH measurements using Beckman-Access immunoassays. Lim SK, Pilon A, Guéchot J. Ann Endocrinol (Paris). 2017 Jul;78(3):186-187. doi: 10.1016/j.ando.2016.08.001. Epub 2017 Feb 13. PMID: 28209262
2017 – CHB
- Impact of country of birth on genetic testing of metastatic lung adenocarcinomas in France: African women exhibit a mutational spectrum more similar to Asians than to Caucasians. Saffroy R, Morère JF, Bosselut N, Innominato PF, Hamelin J, Trédaniel J, Masse S, Dussaule-Duchatelle V, Balaton A, Validire P, Guettier C, Bouchahda M, Lemoine A. Oncotarget. 2017 Feb 7;8(31):50792-50803. doi: 10.18632/oncotarget.15132. eCollection 2017 Aug 1. PMID: 28881604
- Pharmacogenetic determinants of outcomes on triplet hepatic artery infusion and intravenous cetuximab for liver metastases from colorectal cancer (European trial OPTILIV, NCT00852228). Lévi F, Karaboué A, Saffroy R, Desterke C, Boige V, Smith D, Hebbar M, Innominato P, Taieb J, Carvalho C, Guimbaud R, Focan C, Bouchahda M, Adam R, Ducreux M, Milano G, Lemoine A. Br J Cancer. 2017 Sep 26;117(7):965-973. doi: 10.1038/bjc.2017.278. Epub 2017 Aug 17. PMID: 28817838
- Tumor regression grades, K-RAS mutational profile and c-MET in colorectal liver metastases. Lorenzon L, Ricca L, Pilozzi E, Lemoine A, Riggio V, Giudice MT, Mallel G, Fochetti F, Balducci G. Pathol Res Pract. 2017 Aug;213(8):1002-1009. doi: 10.1016/j.prp.2017.04.013. Epub 2017 Apr 21. PMID: 28559118
- EGFR and KRAS molecular genotyping for pulmonary carcinomas: Feasibility of a simple and rapid technique implementable in any department of pathology. Thomas De Montpréville V, Ghigna MR, Lacroix L, Lemoine A, Besse B, Mercier O, Fadel É, Dorfmuller P, Le Chevalier T; Institut d’Oncologie Thoracique. Pathol Res Pract. 2017 Jul;213(7):793-798. doi: 10.1016/j.prp.2017.03.011. Epub 2017 Mar 30. PMID: 28554746
- MET exon 14 mutations as targets in routine molecular analysis of primary sarcomatoid carcinoma of the lung. Saffroy R, Fallet V, Girard N, Mazieres J, Sibilot DM, Lantuejoul S, Rouquette I, Thivolet-Bejui F, Vieira T, Antoine M, Cadranel J, Lemoine A, Wislez M. Oncotarget. 2017 Jun 27;8(26):42428-42437. doi: 10.18632/oncotarget.16403. PMID: 28418914
- Multi-factorial modulation of colorectal carcinoma cells motility – partial coordination by the tetraspanin Co-029/tspan8. Zhu Y, Ailane N, Sala-Valdés M, Haghighi-Rad F, Billard M, Nguyen V, Saffroy R, Lemoine A, Rubinstein E, Boucheix C, Greco C. Oncotarget. 2017 Apr 18;8(16):27454-27470. doi: 10.18632/oncotarget.16247. PMID: 28418857
- Characteristics and Outcomes of Patients with Lung Cancer Harboring Multiple Molecular Alterations: Results from the IFCT Study Biomarkers France. Guibert N, Barlesi F, Descourt R, Léna H, Besse B, Beau-Faller M, Mosser J, Pichon E, Merlio JP, Ouafik L, Guichard F, Mastroianni B, Moreau L, Wdowik A, Sabourin JC, Lemoine A, Missy P, Langlais A, Moro-Sibilot D, Mazières J. J Thorac Oncol. 2017 Jun;12(6):963-973. doi: 10.1016/j.jtho.2017.02.001. Epub 2017 Feb 9. PMID: 28189832
2016 – FACULTE pharMacie
- Localized Mechanical Stress Promotes Microtubule Rescue. de Forges H, Pilon A, Cantaloube I, Pallandre A, Haghiri-Gosnet AM, Perez F, Poüs C. Curr Biol. 2016 Dec 19;26(24):3399-3406. doi: 10.1016/j.cub.2016.10.048. Epub 2016 Dec 1. PMID: 27916523
- Cancer-Related Functions and Subcellular Localizations of Septins. Poüs C, Klipfel L, Baillet A. Front Cell Dev Biol. 2016 Nov 8;4:126. doi: 10.3389/fcell.2016.00126. eCollection 2016. PMID: 27878118
- Serum proteomic signatures as biomarkers of primary biliary cirrhosis diagnosis and prognosis. Baudin B, Bruneel A, Poupon R, Vaubourdolle M. Ann Biol Clin (Paris). 2016 Oct 1;74(5):607-612. doi: 10.1684/abc.2016.1182. PMID: 27707675
- Liver regeneration following repeated reversible portal vein embolization in an experimental model. Tranchart H, Koffi GM, Gaillard M, Lainas P, Poüs C, Gonin P, Nguyen TH, Dubart-Kupperschmitt A, Dagher I. Br J Surg. 2016 Aug;103(9):1209-19. doi: 10.1002/bjs.10153. Epub 2016 Jun 3. PMID: 27256140
- MAPping the Wnt pathway to hepatocellular carcinoma recurrence. Benoit B, Poüs C. Gut. 2016
Sep;65(9):1397-400. doi: 10.1136/gutjnl-2016-311637. Epub 2016 May 17. PMID: 27196583
2016 – CHB
- Mutations at the splice sites of exon 14 of MET gene: a new target for sarcomatoid carcinomas? Wislez M, Domblides C, Cortot A, Lemoine A. Ann Transl Med. 2016 Mar;4(5):96. doi: 10.21037/atm.2016.01.12. PMID: 27047955
- Evidence of intermetastatic heterogeneity for pathological response and genetic mutations within colorectal liver metastases following preoperative chemotherapy. Sebagh M, Allard MA, Bosselut N, Dao M, Vibert E, Lewin M, Lemoine A, Cherqui D, Adam R, Sa Cunha A. Oncotarget. 2016 Apr 19;7(16):21591-600. doi: 10.18632/oncotarget.7809. PMID: 26943031
- Guidelines for the use and interpretation of assays for monitoring autophagy (3rd edition). Klionsky DJ …, Lemoine A et al. Autophagy. 2016 12(1):1-222. doi: 10.1080/15548627.2015.1100356. PMID: 26799652
- Routine molecular profiling of patients with advanced non-small-cell lung cancer: results of a 1-year nationwide programme of the French Cooperative Thoracic Intergroup (IFCT). Barlesi F, Mazieres J, Merlio JP, Debieuvre D, Mosser J, Lena H, Ouafik L, Besse B, Rouquette I, Westeel V, Escande F, Monnet I, Lemoine A, Veillon R, Blons H, Audigier-Valette C, Bringuier PP, Lamy R, Beau-Faller M, Pujol JL, Sabourin JC, Penault-Llorca F, Denis MG, Lantuejoul S, Morin F, Tran Q, Missy P, Langlais A, Milleron B, Cadranel J, Soria JC, Zalcman G; Biomarkers France contributors. Lancet. 2016 Apr 2;387(10026):1415-1426. doi: 10.1016/S0140-6736(16)00004-0. Epub 2016 Jan 15. PMID: 26777916
- Three Rounds of External Quality Assessment in France to Evaluate the Performance of 28 Platforms for Multiparametric Molecular Testing in Metastatic Colorectal and Non-Small Cell Lung Cancer. Dequeker EM, Keppens C, Egele C, Delen S, Lamy A, Lemoine A, Sabourin JC, Andrieu C, Ligtenberg M, Fetique D, Tops B, Descarpentries C, Blons H, Denoux Y, Aube C, Penault-Llorca F, Hofman P, Leroy K, Le Marechal C, Doucet L, Duranton-Tanneur V, Pedeutour F, Soubeyran I, Côté JF, Emile JF, Vignaud JM, Monhoven N, Haddad V, Laurent-Puig P, van Krieken H, Nowak F, Lonchamp E, Bellocq JP, Rouleau E. J Mol Diagn. 2016 Mar;18(2):205-14. doi: 10.1016/j.jmoldx.2015.09.004. Epub 2016 Jan 2. PMID: 26752307
2015 – FACULTE pharMacie
- Septin cooperation with tubulin polyglutamylation contributes to cancer cell adaptation to taxanes. Froidevaux-Klipfel L, Targa B, Cantaloube I, Ahmed-Zaïd H, Poüs C, Baillet A. Oncotarget. 2015 Nov 3;6(34):36063-80. doi: 10.18632/oncotarget.5373. PMID: 26460824
- MALDI-TOF MS applied to apoC-III glycoforms of patients with congenital disorders affecting O-glycosylation. Comparison with two-dimensional electrophoresis. Yen-Nicolaÿ S, Boursier C, Rio M, Lefeber DJ, Pilon A, Seta N, Bruneel A. Proteomics Clin Appl. 2015 Aug;9(7-8):787-93. doi: 10.1002/prca.201400187. Epub 2015 Mar 24. PMID: 25641685
- Red blood cell Thomsen-Friedenreich antigen expression and galectin-3 plasma concentrations in Streptococcus pneumoniae-associated hemolytic uremic syndrome and hemolytic anemia. Burin des Roziers N, Chadebech P, Bodivit G, Guinchard E, Bruneel A, Dupré T, Chevret L, Jugie M, Gallon P, Bierling P, Noizat-Pirenne F. Transfusion. 2015 Jun;55(6 Pt 2):1563-71. doi: 10.1111/trf.12981. Epub 2014 Dec 30. PMID: 25556575
- Thermosensitive and mucoadhesive pluronic-hydroxypropylmethylcellulose hydrogel containing the mini-CD4 M48U1 is a promising efficient barrier against HIV diffusion through macaque cervicovaginal mucus. Bouchemal K, Aka-Any-Grah A, Dereuddre-Bosquet N, Martin L, Lievin-Le-Moal V, Le Grand R, Nicolas V, Gibellini D, Lembo D, Poüs C, Koffi A, Ponchel G. Antimicrob Agents Chemother. 2015 Apr;59(4):2215-22. doi: 10.1128/AAC.03503-14. Epub 2015 Feb 2. PMID: 25645853
2015 – CHB
- Common cancer-associated PIK3CA activating mutations rarely occur in Langerhans cell histiocytosis. Héritier S, Saffroy R, Radosevic-Robin N, Pothin Y, Pacquement H, Peuchmaur M, Lemoine A, Haroche J, Donadieu J, Emile JF. Blood. 2015 Apr 9;125(15):2448-9. doi: 10.1182/blood-2015-01-625491. PMID: 25858893
- Ischemic Postconditioning of the Liver Graft in Adult Liver Transplantation. Ricca L, Lemoine A, Cauchy F, Hamelin J, Sebagh M, Esposti DD, Salloum C, Vibert E, Balducci G, Azoulay D. Transplantation. 2015 Aug;99(8):1633-43. doi: 10.1097/TP.0000000000000685. PMID: 25856406
- Human enhancer of filamentation 1-induced colorectal cancer cell migration: Role of serine phosphorylation and interaction with the breast cancer anti-estrogen resistance 3 protein. Ibrahim R, Lemoine A, Bertoglio J, Raingeaud J. Int J Biochem Cell Biol. 2015 Jul;64:45-57. doi: 10.1016/j.biocel.2015.03.014. Epub 2015 Mar 25. PMID: 25817040
- Comparison of complete pathologic response and hepatic injuries between hepatic arterial infusion and systemic administration of oxaliplatin in patients with colorectal liver metastases. Allard MA, Sebagh M, Baillie G, Lemoine A, Dartigues P, Faitot F, Faron M, Boige V, Vitadello F, Vibert E, Elias D, Adam R, Goéré D, Sa Cunha A. Ann Surg Oncol. 2015 22(6):1925-32. doi: 10.1245/s10434-014-4272-7. Epub 2014 Dec 2. PMID: 25448804
- Mitochondrial Proteins (e.g., VDAC, Bcl-2, HK, ANT) as Major Control Points in Oncology. Brenner C, Lemoine A. Front Oncol. 2014 Dec 15;4:365. doi: 10.3389/fonc.2014.00365. eCollection 2014. PMID: 25566503
Collaborations et partenariats
En construction…








